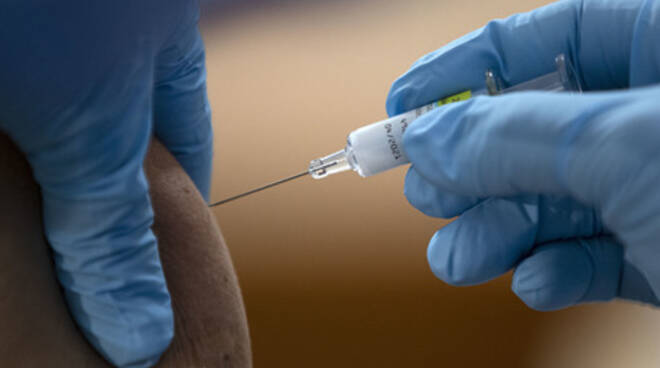
Il vaccino anti Covid di Pfizer/BioNTech, di cui la Gran Bretagna ha avviato ieri – Primo Paese al mondo – la somministrazione su alcune migliaia di persone, è stato “ben tollerato” durante la sperimentazione e non è al centro di alcuna “preoccupazione seria di sicurezza”. Lo ha detto un portavoce della stessa Pfizer citato dai media dopo le notizie sulla reazione allergica non grave manifestata da 2 delle prime persone vaccinate, due operatori sanitari 40enni, e la raccomandazione dell’autorità britannica sui farmaci (Mhra) di non sottoporre a vaccinazione chi abbia “una significativa storia clinica” di allergie alle spalle.
L’autorità nazionale di controllo sui farmaci (Mhra) ha raccomandato – infatti – oggi di non sottoporre a vaccinazione anti Covid chi abbia alle spalle una storia di “significative” reazioni allergiche. L’indicazione è arrivata dopo che due delle centinaia di persone a cui è stato somministrato il vaccino Pfizer/Biontech nel Regno Unito – primo Paese ad aver dato il via ieri alla distribuzione pubblica, dopo il via libera dato nei giorni scorsi dalla stessa Mhra – hanno avuto reazioni allergiche.
“Non voglio pregiudicare il lavoro dei nostri esperti sui vaccini di Pfizer e Moderna, ma posso anticipare che la visione preliminare dei dati che abbiamo ricevuto il primo dicembre è positiva per quanto riguarda efficacia e sicurezza”. Lo afferma la direttrice dell’Ema, Emer Cooke, in un’intervista a Repubblica e ad altri quotidiani internazionali in cui annuncia: “Probabilmente ci esprimeremo il 29 dicembre per Pfizer e il 12 gennaio per Moderna”.
“Dobbiamo ancora controllare la qualità della catena di produzione e la capacità delle aziende di preparare il rimedio su larga scala. Su questi aspetti i nostri esperti hanno domandato informazioni addizionali, così come abbiamo chiesto ulteriori dettagli sulla sicurezza. È uno scambio di informazioni costante, che svolgiamo su base giornaliera”, spiega Cooke, che assicura: “In Europa il processo di autorizzazione è indipendente, non ci sentiamo sotto pressione politica.
La pressione semmai è scientifica perché vogliamo essere certi di fare il meglio per i cittadini”. In merito a possibili effetti collaterali, “con l’autorizzazione predisporremo misure stringenti di monitoraggio su tutta la popolazione, inclusi gli anziani”, sottolinea Cooke.
“I produttori dovranno farci rapporto su qualsiasi evento negativo e ogni mese dovranno inviarci i dati sull’andamento delle vaccinazioni. Così potremo capire se eventuali casi sono legati alla vaccinazione, a particolari”. Chi dovrà ricevere per primo il vaccino “è una decisione che spetta alle autorità nazionali. Ma dobbiamo dire subito che il vaccino non è una bacchetta magica, la popolazione – evidenzia – dovrà continuare a seguire tutte le restrizioni come mascherina, igiene e distanziamento perché all’inizio non ci saranno dosi per tutti e anche dopo, ancora per un certo periodo, fino a quando l’impatto del vaccino non sarà del tutto chiaro”.
Il vaccino AZD1222, sviluppato da AstraZeneca e dall’Università di Oxford, ha mostrato di avere un’efficacia del 62,1% se somministrato in due dosi intere, e del 90% nei volontari che hanno ricevuto mezza dose seguita da una dose intera. E’ quanto emerge dall’analisi provvisoria degli studi di fase III, pubblicata sulla rivista Lancet. Il vaccino è risultato efficace nel prevenire la malattia Covid-19, senza casi gravi e senza ricoveri oltre 21 giorni dopo la prima iniezione.